Die 12 Hallmarks of Aging: Warum wir altern — und was wir dagegen tun können
Das Wichtigste in Kürze
Die Wissenschaft kennt heute 12 biologische Ursachen des Alterns — die sogenannten Hallmarks of Aging
Die bahnbrechende Studie von López-Otín et al. (2023) in Cell erweiterte die ursprünglichen 9 Hallmarks von 2013 um drei neue: gestörte Makroautophagie, chronische Entzündung und Dysbiose
Die 12 Hallmarks sind in drei Kategorien unterteilt: primäre, antagonistische und integrative Ursachen
Alle Hallmarks sind miteinander vernetzt — wer einen Mechanismus beeinflusst, beeinflusst das gesamte System
Entscheidend: Für jeden Hallmark gibt es wissenschaftlich belegte Interventionsmöglichkeiten — Altern ist kein unveränderbares Schicksal
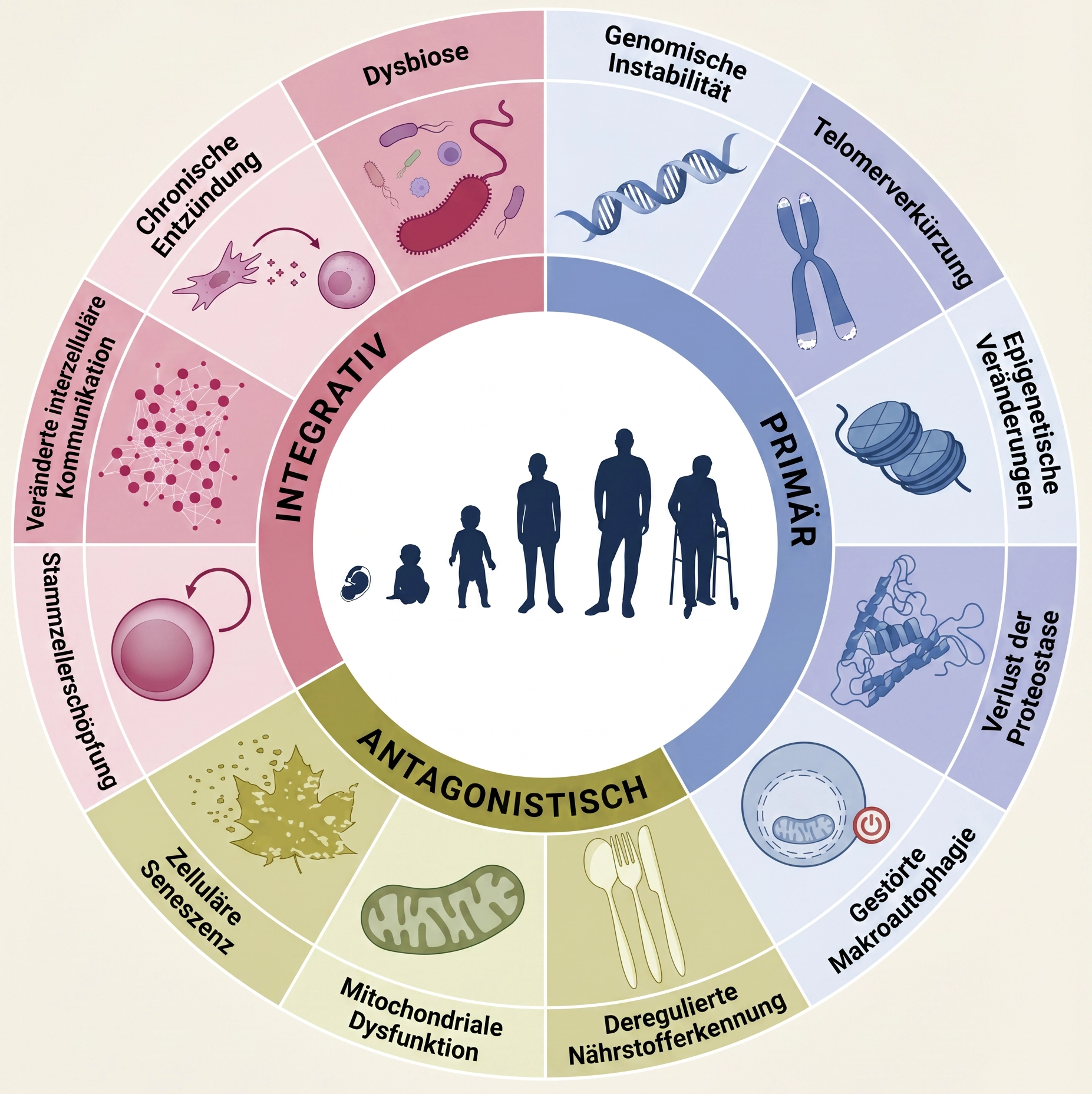
Abbildung: Die 12 Hallmarks of Aging (eigene Darstellung). Basierend auf: López-Otín et al. (2023), Hallmarks of Aging: An Expanding Universe. Cell, 186(2), 243–278. DOI: 10.1016/j.cell.2022.11.001
Einleitung: Altern ist kein Zufall
Warum altern wir? Diese Frage beschäftigt die Menschheit seit Jahrtausenden. Doch erst in den letzten zwei Jahrzehnten hat die Wissenschaft begonnen, die molekularen und zellulären Mechanismen des Alterns systematisch zu entschlüsseln. Ein Meilenstein war die Veröffentlichung der Hallmarks of Aging im Jahr 2013 durch die Forscher Carlos López-Otín, Maria A. Blasco, Linda Partridge, Manuel Serrano und Guido Kroemer im Fachjournal Cell.
Zehn Jahre später — im Januar 2023 — veröffentlichte dasselbe Forscherteam eine aktualisierte Version: „Hallmarks of Aging: An Expanding Universe". Die Studie erweiterte die ursprünglichen neun Hallmarks auf zwölf und integrierte die Erkenntnisse aus fast 300.000 wissenschaftlichen Arbeiten, die seit 2013 zum Thema Altern publiziert worden waren.
Das Ergebnis ist ein umfassendes Rahmenwerk, das erklärt, warum Organismen altern — und, was noch wichtiger ist, wo therapeutische Interventionen ansetzen können. Denn für jeden Hallmark gilt: Er lässt sich nicht nur beschleunigen, sondern auch verlangsamen, aufhalten oder sogar umkehren.
„Altern ist kein passiver Verfall — es ist ein aktiver biologischer Prozess mit identifizierbaren Ursachen und beeinflussbaren Mechanismen."
Die drei Kategorien der Hallmarks
Die 12 Hallmarks of Aging sind nicht gleichrangig. Sie lassen sich in drei Kategorien einteilen, die aufeinander aufbauen.
Primäre Hallmarks sind die molekularen und zellulären Schäden, die den Alterungsprozess auslösen. Dazu gehören genomische Instabilität, Telomerverkürzung, epigenetische Veränderungen, der Verlust der Proteostase und die gestörte Makroautophagie. Sie bilden das Fundament — die eigentlichen Ursachen, aus denen alles Weitere entsteht.
Antagonistische Hallmarks sind zelluläre Reaktionen auf diese Schäden. In jungen Jahren wirken sie schützend, bei chronischer Aktivierung werden sie jedoch selbst zum Problem. Hierzu zählen die deregulierte Nährstofferkennung, die mitochondriale Dysfunktion und die zelluläre Seneszenz.
Integrative Hallmarks sind die systemischen Folgen, die aus der Akkumulation primärer und antagonistischer Schäden entstehen. Sie betreffen den gesamten Organismus: Stammzellerschöpfung, veränderte interzelluläre Kommunikation, chronische Entzündung und Dysbiose.
Diese Hierarchie ist entscheidend: Primäre Hallmarks sind die Auslöser, antagonistische Hallmarks sind die fehlgeleiteten Reaktionen, und integrative Hallmarks sind die systemischen Konsequenzen. Wer Longevity verstehen will, muss alle drei Ebenen kennen.
Die 5 primären Hallmarks
1. Genomische Instabilität (Genomic Instability)
Unsere DNA wird täglich tausendfach beschädigt — durch UV-Strahlung, oxidativen Stress, Umweltgifte und Fehler bei der Zellteilung. Der Körper verfügt über ein ausgeklügeltes Reparatursystem, das diese Schäden normalerweise behebt. Mit zunehmendem Alter verliert dieses System jedoch an Effizienz. Die Folge: Mutationen häufen sich, die Genomstabilität nimmt ab, und das Risiko für Krebs und andere altersbedingte Erkrankungen steigt.
Besonders relevant ist dabei auch die Instabilität der mitochondrialen DNA (mtDNA), die weniger gut geschützt ist als die Kern-DNA und keine vergleichbaren Reparaturmechanismen besitzt.
Relevanz für Longevity: Strategien zur Unterstützung der DNA-Reparatur — etwa durch Ernährung (z. B. NAD+-Vorstufen), Stressreduktion und Vermeidung von Umweltgiften — können die genomische Stabilität fördern.
2. Telomerverkürzung (Telomere Attrition)
Telomere sind die Schutzkappen an den Enden unserer Chromosomen — vergleichbar mit den Plastikkappen an Schnürsenkeln. Bei jeder Zellteilung werden sie kürzer. Wenn sie eine kritische Länge unterschreiten, kann sich die Zelle nicht mehr teilen und geht in den Zustand der Seneszenz über oder stirbt ab.
Das Enzym Telomerase kann Telomere verlängern, ist aber in den meisten adulten Zellen kaum aktiv. Die Telomerlänge gilt heute als einer der wichtigsten Biomarker für biologisches Alter.
Relevanz für Longevity: Regelmässige Bewegung, Stressmanagement, ausreichend Schlaf und eine entzündungshemmende Ernährung können die Telomerverkürzung verlangsamen. Studien zeigen, dass Meditation und bestimmte Lebensstiländerungen die Telomerase-Aktivität erhöhen können.
3. Epigenetische Veränderungen (Epigenetic Alterations)
Die Epigenetik bestimmt, welche Gene in einer Zelle aktiv sind und welche nicht — ohne die DNA-Sequenz selbst zu verändern. Mit dem Alter kommt es zu Veränderungen in der DNA-Methylierung, der Histonmodifikation und der Chromatinstruktur. Diese epigenetischen Veränderungen führen dazu, dass Gene, die eigentlich stumm sein sollten, aktiviert werden — und umgekehrt.
Die sogenannten epigenetischen Uhren (z. B. die Horvath-Uhr) nutzen DNA-Methylierungsmuster, um das biologische Alter einer Person zu bestimmen — oft mit erstaunlicher Genauigkeit.
Relevanz für Longevity: Die Epigenetik ist einer der vielversprechendsten Ansatzpunkte der Longevity-Forschung, weil epigenetische Veränderungen grundsätzlich reversibel sind. Ernährung, Bewegung, Fasten und bestimmte Substanzen (z. B. Resveratrol, Spermidine) können epigenetische Muster positiv beeinflussen.
4. Verlust der Proteostase (Loss of Proteostasis)
Proteine sind die Arbeitspferde unserer Zellen. Damit sie funktionieren, müssen sie korrekt gefaltet und bei Bedarf abgebaut werden. Das Proteostase-Netzwerk — bestehend aus Chaperonen, dem Ubiquitin-Proteasom-System und der Autophagie — sorgt für diese Qualitätskontrolle.
Mit dem Alter lässt die Effizienz dieses Systems nach. Fehlgefaltete Proteine akkumulieren und bilden toxische Aggregate — ein Prozess, der bei neurodegenerativen Erkrankungen wie Alzheimer und Parkinson eine zentrale Rolle spielt.
Relevanz für Longevity: Intervallfasten, Kalorienrestriktion und Substanzen wie Spermidine können die Proteostase unterstützen, indem sie die zelluläre Autophagie aktivieren.
5. Gestörte Makroautophagie (Disabled Macroautophagy) — NEU seit 2023
Die Makroautophagie ist das zelluläre Recyclingprogramm: Beschädigte Organellen, fehlgefaltete Proteine und andere zelluläre Abfallprodukte werden in Membranvesikel (Autophagosomen) eingeschlossen und in Lysosomen abgebaut. Dieser Prozess ist essenziell für die zelluläre Gesundheit.
In der Erstausgabe von 2013 wurde die Autophagie noch als Teilaspekt der Proteostase behandelt. Die Forschung der letzten Dekade hat jedoch gezeigt, dass die Makroautophagie weit mehr als nur Proteine betrifft — sie kann ganze Organellen (z. B. defekte Mitochondrien) und nicht-proteinhaltige Makromoleküle abbauen. Deshalb wurde sie 2023 als eigenständiger Hallmark eingeführt.
Relevanz für Longevity: Fasten und Kalorienrestriktion sind die stärksten natürlichen Aktivatoren der Autophagie. Auch körperliche Aktivität und bestimmte Nahrungsergänzungsmittel (Spermidine, Resveratrol) können die Autophagie fördern.
Die 3 antagonistischen Hallmarks
6. Deregulierte Nährstofferkennung (Deregulated Nutrient-Sensing)
Der Körper verfügt über ein komplexes Netzwerk von Signalwegen, die den Nährstoffstatus erkennen und die zelluläre Aktivität entsprechend anpassen. Zu den wichtigsten gehören der Insulin/IGF-1-Signalweg, mTOR, AMPK und die Sirtuine.
Bei ständiger Nährstoffverfügbarkeit — wie sie in modernen Gesellschaften üblich ist — werden wachstumsfördernde Signalwege (Insulin/IGF-1, mTOR) chronisch aktiviert. Dies beschleunigt das Altern. Umgekehrt aktivieren Nährstoffmangel-Signale (AMPK, Sirtuine) schützende Mechanismen wie Autophagie und DNA-Reparatur.
Relevanz für Longevity: Kalorienrestriktion, Intervallfasten und eine pflanzenbasierte Ernährung können die Nährstoffsensor-Signalwege in Richtung Langlebigkeit verschieben. Die Substanz Rapamycin (mTOR-Inhibitor) ist einer der am besten untersuchten pharmakologischen Ansätze in der Longevity-Forschung.
7. Mitochondriale Dysfunktion (Mitochondrial Dysfunction)
Mitochondrien sind die Kraftwerke der Zelle. Sie produzieren den Grossteil der zellulären Energie in Form von ATP. Mit dem Alter nimmt die mitochondriale Funktion ab: Die Energieproduktion sinkt, die Produktion reaktiver Sauerstoffspezies (ROS) steigt, und die Kommunikation zwischen Mitochondrien und dem Zellkern wird gestört.
Defekte Mitochondrien können zudem entzündungsfördernde Signale aussenden und so zur chronischen Entzündung (Inflammaging) beitragen.
Relevanz für Longevity: Regelmässige Ausdauer- und Krafttraining sind die effektivsten Massnahmen zur Verbesserung der mitochondrialen Funktion. Auch Kälteexposition, NAD+-Vorstufen (NMN, NR) und CoQ10 werden in der Forschung untersucht.
8. Zelluläre Seneszenz (Cellular Senescence)
Seneszente Zellen haben aufgehört, sich zu teilen — aber sie sterben nicht ab. Stattdessen verbleiben sie im Gewebe und sezernieren einen Cocktail aus entzündungsfördernden Molekülen, den sogenannten Senescence-Associated Secretory Phenotype (SASP).
In jungen Jahren ist die Seneszenz ein Schutzmechanismus: Sie verhindert, dass geschädigte Zellen sich unkontrolliert vermehren (Krebsschutz). Im Alter jedoch akkumulieren seneszente Zellen und treiben durch den SASP chronische Entzündungen, Gewebeschäden und Organfunktionsverlust voran.
Relevanz für Longevity: Die Entwicklung von Senolytika — Substanzen, die gezielt seneszente Zellen eliminieren — ist eines der heissesten Forschungsfelder der Longevity-Medizin. Natürliche Senolytika wie Quercetin und Fisetin werden intensiv untersucht.
Die 4 integrativen Hallmarks
9. Stammzellerschöpfung (Stem Cell Exhaustion)
Stammzellen sind für die Regeneration und Erneuerung von Geweben verantwortlich. Mit dem Alter nimmt die Anzahl und Funktionsfähigkeit der Stammzellen in praktisch allen Geweben ab — im Knochenmark, im Darm, im Gehirn, in der Haut.
Diese Erschöpfung der Stammzellen ist eine direkte Konsequenz der primären und antagonistischen Hallmarks: DNA-Schäden, Telomerverkürzung, epigenetische Veränderungen und chronische Entzündung schädigen die Stammzellen und ihre Nische.
Relevanz für Longevity: Stammzelltherapien, Blutplasma-Austausch und Strategien zur Verjüngung der Stammzellnische sind aktive Forschungsgebiete. Im Alltag unterstützen Bewegung, guter Schlaf und eine nährstoffreiche Ernährung die Stammzellfunktion.
10. Veränderte interzelluläre Kommunikation (Altered Intercellular Communication)
Zellen kommunizieren ständig miteinander — über Hormone, Neurotransmitter, Zytokine und extrazelluläre Vesikel. Im Alter wird diese Kommunikation zunehmend gestört: Entzündungssignale nehmen zu, Wachstumsfaktoren nehmen ab, und die neurohormonelle Regulation wird dysreguliert.
Diese veränderte Kommunikation betrifft nicht nur einzelne Gewebe, sondern den gesamten Organismus — sie ist ein Grund dafür, warum Altern ein systemischer Prozess ist.
Relevanz für Longevity: Entzündungshemmende Ernährung, Stressreduktion, soziale Einbindung und regelmässige Bewegung können die interzelluläre Kommunikation positiv beeinflussen.
11. Chronische Entzündung (Chronic Inflammation) — NEU seit 2023
Inflammaging — die Kombination aus Inflammation und Aging — beschreibt den Zustand einer niedriggradigen, chronischen, sterilen Entzündung, die mit dem Alter zunimmt. Diese Entzündung wird nicht durch Krankheitserreger ausgelöst, sondern durch interne Signale: seneszente Zellen (SASP), defekte Mitochondrien, Darm-Dysbiose und fehlgefaltete Proteine.
Chronische Entzündung ist ein zentraler Treiber praktisch aller altersbedingten Erkrankungen — von Herz-Kreislauf-Erkrankungen über Diabetes bis hin zu Alzheimer und Krebs.
Relevanz für Longevity: Eine entzündungshemmende Lebensweise — mediterrane Ernährung, Omega-3-Fettsäuren, regelmässige Bewegung, ausreichend Schlaf, Stressmanagement — ist eine der wirksamsten Strategien gegen das Altern. Auch die Messung von Entzündungsmarkern (CRP, IL-6) gehört zu einer modernen Longevity-Diagnostik.
12. Dysbiose (Dysbiosis) — NEU seit 2023
Das Darmmikrobiom — die Gesamtheit aller Mikroorganismen im Darm — spielt eine zentrale Rolle für Gesundheit und Langlebigkeit. Mit dem Alter verändert sich die Zusammensetzung des Mikrobioms: Die Diversität nimmt ab, entzündungsfördernde Bakterien nehmen zu, und die Darmbarriere wird durchlässiger (Leaky Gut).
Diese Dysbiose verstärkt die chronische Entzündung und beeinflusst über die Darm-Hirn-Achse auch die kognitive Funktion und die psychische Gesundheit.
Relevanz für Longevity: Eine ballaststoffreiche, pflanzenbasierte Ernährung, fermentierte Lebensmittel, Probiotika und die Vermeidung unnötiger Antibiotika sind die wichtigsten Massnahmen zur Erhaltung eines gesunden Mikrobioms. Studien an Hundertjährigen in den Blue Zones zeigen, dass ein vielfältiges Mikrobiom mit Langlebigkeit korreliert.
Die Vernetzung: Warum alles zusammenhängt
Ein zentraler Punkt der Studie von López-Otín et al. ist die Erkenntnis, dass die 12 Hallmarks nicht isoliert wirken. Sie sind in einem komplexen Netzwerk miteinander verbunden.
Genomische Instabilität führt zu epigenetischen Veränderungen. Telomerverkürzung aktiviert zelluläre Seneszenz. Seneszente Zellen treiben über den SASP die chronische Entzündung voran. Chronische Entzündung schädigt Stammzellen und beschleunigt deren Erschöpfung. Mitochondriale Dysfunktion verstärkt oxidativen Stress und Entzündung. Dysbiose fördert Entzündung und verändert die interzelluläre Kommunikation.
Diese Vernetzung bedeutet: Wer an einem Punkt ansetzt, beeinflusst das gesamte System. Das ist gleichzeitig die Herausforderung und die Chance der Longevity-Medizin.
Was bedeutet das für die Praxis?
Die 12 Hallmarks of Aging sind kein abstraktes Konzept — sie haben direkte Konsequenzen für die tägliche Gesundheitsvorsorge.
Regelmässige Bewegung wirkt auf mitochondriale Dysfunktion, Stammzellerschöpfung, chronische Entzündung und Telomerverkürzung.
Intervallfasten und Kalorienrestriktion beeinflussen die deregulierte Nährstofferkennung, die gestörte Makroautophagie und den Verlust der Proteostase.
Ausreichend Schlaf unterstützt die genomische Stabilität, reduziert chronische Entzündung und beeinflusst epigenetische Veränderungen positiv. Mehr dazu im Artikel Schlaf und Longevity.
Stressmanagement verlangsamt die Telomerverkürzung, reduziert chronische Entzündung und verbessert die interzelluläre Kommunikation.
Mediterrane Ernährung wirkt gegen Dysbiose, chronische Entzündung und deregulierte Nährstofferkennung. Mehr dazu im Artikel Ernährung und Langlebigkeit.
Soziale Einbindung verbessert die interzelluläre Kommunikation und reduziert chronische Entzündung.
Mehr zu den praktischen Ansätzen der Longevity-Medizin auf der Seite Ansätze.
Dr. Anna Wohlthat über die Hallmarks of Aging
Die 12 Hallmarks of Aging sind ein zentrales Thema in den Vorträgen und Keynotes von Dr. Anna Wohlthat. Als Gesundheitsökonomin und Longevity-Architektin verbindet sie die wissenschaftlichen Erkenntnisse mit praktischen Handlungsempfehlungen — für Unternehmen, Führungskräfte und alle, die verstehen wollen, wie ein langes, gesundes Leben gelingt.
In ihren Keynotes auf Bühnen in ganz Europa — vom Internationalen Expertenkongress in Mastershausen über das EU-Parlament in Brüssel bis hin zu Rotary Clubs in Deutschland und der Schweiz — erklärt Dr. Wohlthat, warum Prävention die beste Investition ist und wie die Hallmarks of Aging den Weg zu einer neuen Gesundheitsarchitektur weisen.
Mehr über Dr. Anna Wohlthat als Speakerin oder Kontakt aufnehmen für eine Keynote-Anfrage.
Fazit: Altern verstehen heisst Altern beeinflussen
Die 12 Hallmarks of Aging sind mehr als eine wissenschaftliche Klassifikation — sie sind eine Landkarte für alle, die das Altern verstehen und aktiv gestalten wollen. Die Forschung zeigt eindeutig: Altern ist kein unveränderbares Schicksal. Es ist ein biologischer Prozess mit identifizierbaren Ursachen — und beeinflussbaren Mechanismen.
Die Frage ist nicht, ob wir altern. Die Frage ist, wie wir altern.
Quellen und weiterführende Literatur
[1] López-Otín, C., Blasco, M.A., Partridge, L., Serrano, M., Kroemer, G. (2013). The Hallmarks of Aging. Cell, 153(6), 1194–1217.
[2] López-Otín, C., Blasco, M.A., Partridge, L., Serrano, M., Kroemer, G. (2023). Hallmarks of Aging: An Expanding Universe. Cell, 186(2), 243–278.
[3] Epel, E.S., Blackburn, E.H., Lin, J. et al. (2004). Accelerated telomere shortening in response to life stress. Proceedings of the National Academy of Sciences, 101(49), 17312–17315.
[4] Xu, M., Pirtskhalava, T., Farr, J.N. et al. (2018). Senolytics improve physical function and increase lifespan in old age. Nature Medicine, 24, 1246–1256.
[5] Wilmanski, T., Diener, C., Rappaport, N. et al. (2021). Gut microbiome pattern reflects healthy ageing and predicts survival in humans. Nature Metabolism, 3, 274–286.

